Hydroxyde de cobalt (ii)est un composé inorganique avec la formule chimique Co (OH) 2, CAS 21041-93-0, et est une poudre de couleur bleu clair ou rose. Insoluble dans l'eau, légèrement amphotérique, difficile à dissoudre dans des bases fortes, mais solubles dans les solutions de sel acide et ammonium. Principalement utilisé comme agent de coloriage pour le verre et l'émail, une matière première pour produire d'autres composés de cobalt et un dessicant pour le vernis et les revêtements. Il dispose d'un large éventail d'applications dans le domaine de l'électrocatalyse. Par exemple, il peut être utilisé comme électrocatalyseur d'évolution de l'hydrogène cathode pour produire de l'hydrogène gazier à haute pureté en électrolysant l'eau. Les chercheurs ont conçu et préparé avec succès un réseau de nano-tôles composite nano-nano-nano-nano-sheet en hydroxyde de cobalt supporté sur un substrat de nickel en mousse poreuse comme électrocatalyste de l'évolution de l'hydrogène cathode du dispositif d'électrolyse d'eau, et étudié ses performances électrochimiques d'hydrogène dans le système alcalin. Cela indique que l'hydroxyde de cobalt a une bonne activité électrochimique et une bonne stabilité.

|
Formule chimique |
COH2O2 |
|
Masse exacte |
93 |
|
Poids moléculaire |
93 |
|
m/z |
93 (100.0%) |
|
Analyse élémentaire |
CO, 63,41; H, 2.17; O, 34.43 |
|
|
|

Méthode de synthèse deHydroxyde de cobalt (ii):
1. Méthode de synthèse: Méthode des déchets contenant du cobalt Divers déchets contenant du cobalt est dissous par l'acide nitrique et l'acide chlorhydrique. La solution de chlorure de cobalt obtenue est purifiée avec du peroxyde d'hydrogène pour éliminer le fer. Si nécessaire, du carbonate de sodium ou de l'eau d'ammoniac est ajouté pour assurer une purification complète. La solution de chlorure de cobalt purifiée est ajoutée avec l'hydroxyde de sodium pour produire de l'hydroxyde de cobalt, qui est ensuite lavée et centrifugé pour produire des produits d'hydroxyde de cobalt.
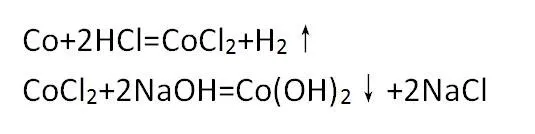
2. Méthode d'électrolyse: Il est obtenu par électrolyse de la solution saline avec du cobalt comme anode.
3. Le sulfate ou le nitrate de cobalt divalent réagit avec l'alcali pour produire de l'hydroxyde de cobalt. Dissoudre 100g coso4 · 7H2O Dans l'eau pour former une solution presque saturée. Ajouter 42 g d'hydroxyde de sodium dans 60 ml d'eau pour former une solution alcaline à condition de chauffage et d'agitation continue. La réaction de précipitation est réalisée dans un long bécher, ce qui est propice à la clarification du mélange. Le précipité formé au début est bleu. Lorsqu'il est chauffé sur un bain-marie, le précipité devient rapidement rouge. Après clarification, décantant et lavez à l'eau pendant plusieurs fois, puis filtrez sur l'entonnoir Buchner et lavez à l'eau jusqu'à ce que l'eau de lavage soit neutre. Enfin, il est séché dans un séchoir à vide équipé de H concentré2DONC4. Étant donné que l'hydroxyde de cobalt sera lentement oxydé dans l'air, l'opération de préparation est mieux effectuée dans une boîte d'opération protégée par le gaz inerte.
4. Utilisez du cobalt métallique pour réagir avec l'acide nitrique dilué à la température de 60 ~ 70 degrés. Lorsque la réaction s'arrête essentiellement, complétez l'eau perdue, séparez l'excès de métal, ajoutez Coco3Pour rendre la solution près du neutre, et maintenez-la à cette température pendant 2 ~ 3H, filtrez et retirez la matière insoluble. Ensuite, ajoutez lentement 2% d'ammoniac à la condition d'agitation et de chauffage continu, afin que le précipité bleu qui commence à se former puisse être transformé en violet dans le temps, puis en précipité rouge rose. Une fois la réaction terminée et clarifiée, aspirez la solution avec une paille, lavez-la avec de l'eau jusqu'à ce que la solution aqueuse soit neutre, filtrez rapidement les sédiments et séchez-la dans un séchoir à vide équipé de H concentré H2DONC4.


Hydroxyde de cobalt (ii)(CO (OH) 2) est un composé inorganique avec plusieurs applications importantes. Principalement utilisé comme matières premières pour la production de sel de cobalt, comme dessiccants pour les revêtements et les vernis, comme liquides saturés pour les batteries, et comme agents de coloration pour l'industrie de l'émail en verre. Dans le domaine de l'électrocatalyse, l'hydroxyde de cobalt est également utilisé comme catalyseur.
Applications dans l'industrie chimique

(1) Colorants pour le verre et l'émail
En raison de sa couleur vive et de sa résistance à la décoloration, il est souvent utilisé comme agent de coloriage pour le verre et l'émail. Dans le processus de fabrication du verre, l'ajout d'une quantité appropriée de cette substance peut donner au verre une couleur spécifique, augmenter l'esthétique et la valeur ajoutée du produit. De même, dans la fabrication de l'émail, il est également utilisé comme agent de coloriage pour donner aux produits en émail une couleur plus riche.
(2) matières premières pour produire d'autres composés de cobalt
Il s'agit d'une matière première importante pour produire d'autres composés de cobalt. Grâce à des réactions chimiques, l'hydroxyde de cobalt peut être converti en autres sels de cobalt ou oxydes de cobalt, tels que le chlorure de cobalt, le sulfate de cobalt, l'oxyde de cobalt, etc.


(3) dessiccants pour les peintures et les vernis
Dans l'industrie de la peinture et du vernis, il est couramment utilisé comme dessiccant. Il peut accélérer le processus de séchage des revêtements et des vernis, améliorant l'efficacité de la production et la qualité des produits. L'effet de séchage est obtenu par son hygroscopicité et son activité chimique, qui peut absorber l'humidité et les composés organiques volatils dans les revêtements et les vernis, favorisant le durcissement et le séchage des revêtements.
Application dans le domaine de la nouvelle énergie
(1) Matériaux de la batterie
Il dispose d'un large éventail d'applications dans le domaine des batteries. Il s'agit de l'une des matières premières importantes pour les batteries secondaires telles que les batteries lithium-ion et les batteries d'hydrogène nickel. Dans les batteries au lithium-ion, il peut être utilisé comme matière première pour les matériaux d'électrode positifs, en réagissant avec des ions lithium pour obtenir le processus de charge et de décharge de la batterie. Dans les batteries d'hydrogène nickel, en tant qu'additif pour les matériaux d'électrode négatifs, il peut améliorer la stabilité du cycle et la capacité de la batterie.
Avec le développement rapide de nouveaux véhicules énergétiques et la technologie de stockage d'énergie, la demande de batteries hautes performances augmente constamment. En tant que composant important des matériaux de la batterie, sa demande du marché se développe également en permanence.


(2) catalyseurs dans le domaine de l'électrocatalyse
Il dispose d'un large éventail d'applications dans le domaine de l'électrocatalyse, comme servir d'électrocatalyste d'évolution de l'hydrogène cathode pour la production d'hydrogène de gaz à haute pureté à partir de l'électrolyse d'eau. Les chercheurs ont conçu et préparé avec succès un réseau de nano-tôles composite nano-nano-nano-nano-sheet en hydroxyde de cobalt supporté sur un substrat de nickel en mousse poreuse comme électrocatalyste de l'évolution de l'hydrogène cathode du dispositif d'électrolyse d'eau, et étudié ses performances électrochimiques d'hydrogène dans le système alcalin. Cela indique qu'il a une bonne activité électrochimique et stabilité, et peut être utilisé comme électrocatalyste efficace.
Applications dans d'autres domaines
(1) Fabrication en céramique
Il est également appliqué dans la fabrication en céramique. Il peut servir d'agent de coloriage et d'additif pour la céramique, dominant des produits en céramique avec des couleurs et des propriétés spécifiques. En ajoutant cette substance, les produits en céramique peuvent avoir des couleurs plus riches et une dureté plus élevée, améliorer la qualité des produits et la valeur ajoutée.
(2) colorants et pigments
Il peut également être utilisé pour fabriquer certains pigments et colorants bleus ou violets. Ces pigments et colorants ont une large gamme d'applications dans les champs de textiles, d'impression, de revêtements, etc., et peuvent donner des couleurs et des motifs spécifiques aux produits.


(3) catalyseur
En plus de son application dans le domaine de l'électrocatalyse, il peut également servir de catalyseur pour d'autres réactions chimiques. Par exemple, il peut servir de catalyseur pour la décomposition du peroxyde d'hydrogène, accélérant le processus et production d'oxygène et d'eau. Ce catalyseur a une valeur d'application potentielle dans des champs tels que la protection de l'environnement et le traitement de l'eau.
(4) Matériaux magnétiques
Il a un certain degré de magnétisme, il peut donc être utilisé comme l'une des matières premières pour les matériaux magnétiques. En composant ou en dopage avec d'autres matériaux magnétiques, des matériaux composites avec des propriétés magnétiques spécifiques peuvent être préparées pour une utilisation dans des champs tels que l'enregistrement magnétique et la détection magnétique.
(5) Autres utilisations
Il peut également être utilisé pour préparer d'autres composés de cobalt, tels que les oxydes de cobalt, les sulfures, etc. Ces composés ont une large gamme d'applications dans des champs tels que l'électronique, l'optique et les capteurs. De plus, l'hydroxyde de cobalt peut également être utilisé pour préparer certains produits chimiques et médicaments spéciaux, tels que les médicaments anti-cancer.


Deux phases cristallines de l'hydroxyde de cobalt:
1. A-co (OH) 2 a une structure similaire à celle de l'hydrotalcite, et sa caractéristique typique est la structure de l'oxyde de métal composite dihydroxy en couches. En raison de sa grande structure en couches, sa conductivité est bonne. Ce type d'hydroxyde de cobalt est généralement de couleur bleu-vert. Cependant, cette phase est instable et à l'état métastable, ce qui est facile à changer en phase.
2, - CO (OH) 2 a une structure de brucite, les ions hydroxyle sont hexagonaux étroitement emballés et les cations remplissent tous les espaces octaédriques entre chaque deux ions hydroxyle adjacents; La couche structurelle qui forme l'ocaédre de coordination. Il y a des liaisons ioniques dans les couches structurelles et les couches structurelles sont maintenues par phases. Sa couleur est souvent en rouge brique ou en rouge rose.
Le cobalt est un élément important en biologie. Une petite dose peut activer de nombreuses enzymes qui régulent la respiration tissulaire, l'hématopoïèse et d'autres processus. À une grande dose, il inhibe l'activité de ces enzymes, affecte le métabolisme des glucides, endommage sélectivement la partie endocrinienne du pancréas, affecte le système cardiovasculaire, dilate les vaisseaux sanguins, réduit la pression artérielle et endommage sélectivement le myocarde. L'inhalation de composés de cobalt entraîne parfois un asthme bronchique. Les composés de cobalt moulants peuvent provoquer une dermatite aiguë et parfois former des ulcères à la surface. La concentration maximale admissible de métal de cobalt etHydroxyde de cobalt (ii)est 0. 5 mg / m ³. Les masques à gaz, les vêtements de travail résistants à la poussière et les gants de protection doivent être utilisés pendant le travail pour protéger les organes respiratoires et la peau. Lorsqu'il est exposé à la poussière de cobalt métallique au travail, il est recommandé de se laver les mains avec une pâte. Faites attention à la prévention des poussières et à l'élimination de la poussière en production et adoptez un fonctionnement humide.
étiquette à chaud: COBALT (II) Hydroxyde Cas 21041-93-0, fournisseurs, fabricants, usine, gros, acheter, prix, vrac, à vendre








