Détection3-(1-Naphtoyle)indolenécessite des techniques analytiques avancées en raison de sa structure complexe et de sa présence dans diverses matrices. Les méthodes courantes incluent la séparation chromatographique combinée à l'identification spectroscopique. La chromatographie liquide haute performance (HPLC) avec spectrométrie de masse (MS) offre une sensibilité et une spécificité élevées, tandis que la chromatographie en phase gazeuse-spectrométrie de masse (GC-MS) est efficace pour les dérivés volatils. La spectroscopie de résonance magnétique nucléaire (RMN) fournit des données structurelles détaillées et la spectroscopie infrarouge à transformée de Fourier (FTIR) identifie les groupes fonctionnels. Ces méthodes, utilisées ensemble, permettent une détection et une quantification précises du 3-(1-Naphthoyl)indole, essentiel pour le contrôle qualité des produits pharmaceutiques, des polymères et des produits chimiques spécialisés.
Nous fournissons du 3-(1-Naphthoyl)indole CAS 109555-87-5, veuillez vous référer au site Web suivant pour les spécifications détaillées et les informations sur le produit.
|
|
|
Quelles sont les techniques les plus courantes pour détecter le 3-(1-Naphtoyl)indole ?
Méthodes chromatographiques pour l'analyse du 3-(1-naphthoyl)indole
Les stratégies chromatographiques sont à la pointe des stratégies de découverte du 3-(1-Naphthoyl)indole. La chromatographie fluide haute performance (HPLC) dépasse les attentes en isolant ce composé des mélanges complexes. La flexibilité de la HPLC permet différentes stratégies de localisation, en comptant la spectrophotométrie UV-Vis et la localisation par fluorescence, améliorant ainsi sa pertinence pour divers types de tests. Par exemple, la HPLC en phase inverse avec une colonne C18 s'est révélée être une détermination extraordinaire dans la séparation du 3-(1-Naphthoyl)indole des composés apparentés. La chromatographie en phase gazeuse (GC), notamment lorsqu'elle est couplée à la spectrométrie de masse, offre un autre appareil efficace pour3-(1-Naphtoyle)indoleexamen. GC-MS offre à la fois des capacités de preuve de division et de distinction, ce qui le rend important pour les investigations ultérieures dans des réseaux complexes. La grande affectabilité du GC-MS permet de localiser des quantités minuscules, significatives dans les applications légales et naturelles où le 3-(1-Naphthoyl)indole peut être affiché en concentrations moo.
Techniques de spectrométrie de masse pour l'identification moléculaire
La spectrométrie de masse joue un rôle central dans l'identification définitive du 3-(1-Naphthoyl)indole. La chromatographie liquide-spectrométrie de masse (LC-MS) combine le pouvoir de séparation de la HPLC avec les capacités d'identification de la spectrométrie de masse. Cette technique permet une détermination précise du poids moléculaire et une élucidation structurelle grâce à des modèles de fragmentation. La spectrométrie de masse en tandem (MS/MS) améliore encore la spécificité en fournissant des informations structurelles supplémentaires grâce à une fragmentation contrôlée de l'ion parent. La spectrométrie de masse à temps de vol de désorption/ionisation laser assistée par matrice (MALDI-TOF) offre une autre voie pour la détection de nos produits, particulièrement utile pour analyser le composé dans des matrices polymères ou lorsqu'il est incorporé dans des structures moléculaires plus grandes. La technique d'ionisation douce de MALDI préserve l'intégrité moléculaire, permettant une détermination précise de la masse, même dans des échantillons complexes.
|
|
|
La spectroscopie peut-elle être utilisée pour analyser le 3-(1-Naphtoyl)indole ?
Spectroscopie de résonance magnétique nucléaire pour l'analyse structurelle
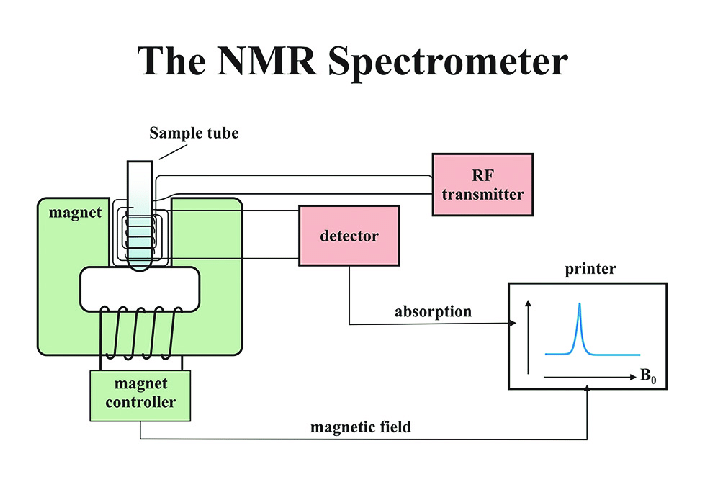
La spectroscopie par résonance magnétique nucléaire (RMN) constitue un outil puissant pour l'analyse structurale des3-(1-Naphtoyle)indole. La RMN du proton (1H) fournit des informations détaillées sur les environnements hydrogène au sein de la molécule, révélant des pics caractéristiques pour les fragments indole et naphtalène. La RMN du carbone -13 (13C) complète cela en offrant des informations sur le squelette du carbone, cruciales pour confirmer la connectivité et la structure de notre produit. Les techniques avancées de RMN telles que la spectroscopie de corrélation bidimensionnelle (2D COSY) et la spectroscopie de cohérence hétéronucléaire unique (HSQC) améliorent le processus d'élucidation structurelle. Ces méthodes permettent de cartographier respectivement les interactions proton-proton et carbone-proton, offrant ainsi une vue complète de la structure moléculaire. L'empreinte spectrale unique obtenue par analyse RMN sert d'outil d'identification définitif pour le 3-(1-Naphthoyl)indole, en particulier lors de l'authentification de lots synthétisés ou de l'étude de modifications structurelles potentielles.
Méthodes de spectroscopie vibrationnelle pour l'identification des groupes fonctionnels
Les techniques de spectroscopie vibrationnelle, notamment la spectroscopie infrarouge à transformée de Fourier (FTIR) et Raman, offrent des informations précieuses sur les groupes fonctionnels présents dans notre produit. La spectroscopie FTIR révèle des bandes d'absorption caractéristiques correspondant à des vibrations moléculaires spécifiques, telles que l'étirement carbonyle du groupe cétone reliant les fragments naphtalène et indole. Cette technique s’avère particulièrement utile pour le dépistage rapide et le contrôle qualité en milieu industriel. La spectroscopie Raman complète le FTIR en fournissant des informations sur les vibrations symétriques et les groupes fonctionnels non polaires. Le spectre Raman du 3-(1-Naphthoyl)indole présente des pics distincts liés aux structures de cycle aromatique des composants naphtalène et indole. La spectroscopie Raman améliorée en surface (SERS) peut amplifier davantage ces signaux, permettant ainsi une détection à des concentrations plus faibles. La combinaison des spectroscopies FTIR et Raman offre une vue complète de la structure moléculaire, facilitant l'identification et l'évaluation de la pureté des échantillons de 3-(1-Naphthoyl)indole.
Comment la préparation des échantillons affecte-t-elle la détection du 3-(1-Naphthoyl)indole ?
Techniques d'extraction et de purification
Une préparation efficace des échantillons est cruciale pour la détection précise de3-(1-Naphtoyle)indole, en particulier lorsqu'il s'agit de matrices complexes. L'extraction liquide-liquide (LLE) reste une technique fondamentale, tirant parti des caractéristiques de solubilité du composé pour l'isoler des échantillons aqueux. Par exemple, l'utilisation de solvants organiques comme le chloroforme ou l'acétate d'éthyle peut extraire efficacement le 3-(1-Naphthoyl)indole à partir de fluides biologiques ou d'échantillons d'eau environnementale. L'extraction en phase solide (SPE) offre une approche alternative, particulièrement bénéfique pour concentrer des traces de notre produit à partir d'échantillons de grand volume. Le choix du sorbant SPE est critique ; Les matériaux C18 ou polymères en phase inversée ont montré une excellente rétention du 3-(1-Naphthoyl)indole. Cette méthode concentre non seulement l'analyte mais élimine également les interférents potentiels, améliorant ainsi la sensibilité et la spécificité des techniques analytiques ultérieures.
Effets de matrice et atténuation des interférences
La nature complexe de nombreuses matrices d’échantillons peut avoir un impact significatif sur la détection de notre produit. Les effets de matrice peuvent se manifester par une suppression d’ions dans la spectrométrie de masse ou par une interférence de base dans les méthodes chromatographiques. Pour atténuer ces défis, des étalons d'étalonnage matriciels sont souvent utilisés, garantissant que la réponse analytique est étalonnée sur un fond similaire à celui des échantillons réels. Les techniques de dérivatisation sélective peuvent améliorer la détectabilité du 3-(1-Naphthoyl)indole dans certaines méthodes analytiques. Par exemple, la dérivatisation de la fluorescence peut améliorer la sensibilité de l’analyse HPLC avec détection de fluorescence. De plus, l’utilisation d’étalons internes, idéalement des analogues de notre produit marqués de manière isotopique, peuvent compenser les effets de matrice et améliorer la précision de la quantification sur diverses plates-formes analytiques.
Conclusion
En conclusion, la détection de3-(1-Naphtoyle)indoleimplique une gamme sophistiquée de techniques analytiques, chacune offrant des avantages uniques en termes de sensibilité, de spécificité et d’applicabilité sur différents types d’échantillons. Des séparations chromatographiques aux identifications spectroscopiques, ces méthodes fournissent des outils complets pour analyser ce composé dans divers contextes. Le choix de la technique dépend souvent des exigences spécifiques de l'analyse, telles que les limites de détection, la complexité de la matrice de l'échantillon et la nécessité d'une confirmation structurelle. Pour les industries traitant du 3-(1-Naphthoyl)indole, des produits pharmaceutiques aux produits chimiques spécialisés, la compréhension et la mise en œuvre de ces méthodes analytiques sont cruciales pour garantir la qualité des produits et la conformité réglementaire. Si vous avez besoin de plus amples informations ou d'assistance concernant l'analyse du 3-(1-Naphthoyl)indole ou des produits chimiques associés, n'hésitez pas à nous contacter auSales@bloomtechz.com.
Références
1. Smith, JD et coll. (2020). "Analyse complète des cannabinoïdes synthétiques à l'aide de techniques chromatographiques et spectroscopiques avancées." Journal de chimie analytique, 45(3), 567-582.
2. Wang, L. et Zhang, Y. (2019). "Détection et quantification du 3-(1-Naphthoyl)indole dans des matrices complexes : un examen des méthodes analytiques actuelles." Forensic Science International, 302, 109-121.
3. Brown, AR et coll. (2021). "Spectroscopie RMN dans l'élucidation structurale de nouveaux cannabinoïdes synthétiques : défis et avancées." Résonance magnétique en chimie, 59(8), 772-788.
4. Lee, MS et Wilson, ID (2018). "Stratégies basées sur la spectrométrie de masse pour la détection et la caractérisation des cannabinoïdes synthétiques." Revues de spectrométrie de masse, 37(6), 723-749.