Amidure de lithiumest une substance chimique de formule chimique LiNH2 et CAS 7782-89-0. C'est une poudre cristalline blanche et brillante avec une odeur d'ammoniac, insoluble dans le kérosène, soluble dans l'ammoniac liquide, soluble dans l'eau froide et fortement hydrolysée lorsqu'elle est exposée à l'eau chaude. Point de fusion de 380 à 400 degrés, point d'ébullition de 430 degrés, densité relative de 1,17817,5. Dissoudre dans l'eau froide, décomposer en hydroxyde de lithium et ammoniac dans l'eau chaude, dissoudre dans l'acide chlorhydrique pour former du chlorure de lithium et du chlorure d'ammonium, légèrement solubles dans l'ammoniac liquide et l'éthanol, insolubles dans l'éther et le benzène. Se décompose lentement dans l'air, mais ne brûle pas. Lorsqu'il est chauffé à 450 degrés sous vide, il se décompose en LiNH3 et NH3. C'est une base forte qui réagit facilement avec le soufre et le sélénium. Facile à oxyder, peut être oxydé par le dioxyde d'azote en azoture de lithium. Réagit avec l'acide chlorhydrique concentré pour générer de l'ammoniac libre. A un léger effet corrosif sur le verre. Principalement utilisé dans la synthèse organique et la fabrication de médicaments, c'est un bon matériau de stockage d'hydrogène avec l'hydrure de lithium et l'imine de lithium.

|
|
|
|
Formule chimique |
H2LiN |
|
Masse exacte |
23 |
|
Poids moléculaire |
23 |
|
m/z |
23 (100.0%), 22 (8.2%) |
|
Analyse élémentaire |
H, 8,78 ; Li, 30.22 ; N, 61h00 |

Amidure de lithiumpeut être utilisé pour l'alkylation des nitriles et des cétones, la synthèse de composés à base d'acétylène, etc. Les exemples d'application sont les suivants :
1. Synthèse du sulfamide chiral.
Les alkyl(aryl)sulfonylamides chiraux ont une importance d'application importante dans la synthèse organique fine et la synthèse de médicaments chiraux. En l'utilisant comme cofacteur chiral, de nombreux composés aminés chiraux et médicaments chiraux difficiles à synthétiser par les voies conventionnelles peuvent être synthétisés de manière asymétrique. La solution technique est la suivante : un procédé de synthèse de sulfonamide chiral, utilisant du thiosulfonamide chiral comme matière première, et sa réduction avec de l'ammoniac liquide aminolithium pour obtenir du sulfonamide chiral. La formule de la réaction est :

Parmi eux, R est l'un des éléments suivants : alkyle en C1 à C10, phényle, paratoluène, ortho méthylphényle, méta méthylphényle, para éthylphényle, para tert butylphényle, para acétyl phényle, ortho acétyl phényle, naphtyle. Les étapes sont les suivantes :
Étape 1 :
Préparer LiNH2 en utilisant du lithium métal et de l'ammoniac liquide ;
Étape 2 :
Ajoutez goutte à goutte LiNH2 à la solution de thiosulfinate chiral, remuez la réaction une fois l'addition goutte à goutte terminée et continuez pendant 2 à 20 heures à une température de réaction de -80 degrés à -80 degrés ;
Étape 3 :
Une fois la réaction terminée, ajouter des glaçons au système et extraire avec du dichlorométhane. Mélanger les phases organiques et éliminer le solvant pour obtenir un solide brun rougeâtre. Recristalliser dans le n-hexane pour obtenir un sulfonamide chiral à valeur ee élevée.
2. Stockage actif au lithium pour les batteries lithium-ion.
Il est utilisé pour réduire les pertes initiales irréversibles et sert de source de lithium universelle pour des matériaux d'électrode et des batteries au lithium, ou de source de lithium universelle pour ceux-ci, un matériau d'alimentation en lithium en poudre présentant un potentiel électrochimique par rapport à Li/Li+ de 0,5 à 2 V étant utilisé comme stockage actif de lithium, choisi parmi l'hydrure de lithium, l'aminolithium, l'iminolithium et l'hydrure de tétralithium-ammonium. Ces composés se décomposent et libèrent du lithium et des sous-produits gazeux lorsqu'ils dépassent le potentiel d'oxydation standard dans leur cellule électrochimique lors de l'application du potentiel correspondant.
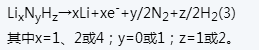

Le lithium amide (LiNH2), en tant que substance chimique importante, a un large éventail d'applications dans de multiples domaines.

Synthèse organique
LiNH2 joue un rôle crucial dans le domaine de la synthèse organique. Ce n'est pas seulement un catalyseur et un réactif pour diverses réactions organiques, mais il favorise également la synthèse de composés organiques complexes.
1. Catalyseurs et réactifs
L'entreprise a mené une analyse de son avantage concurrentiel pour identifier ses forces et ses faiblesses par rapport à ses concurrents.
(1) Promoteur de condensation :
LiNH2 présente d'excellentes performances catalytiques dans les réactions de condensation aldolique et autres réactions de condensation, favorisant une liaison efficace entre les réactifs.
(2) Agent réducteur :
En synthèse organique, LiNH2 est couramment utilisé comme agent réducteur pour participer à diverses réactions redox et aider à la synthèse des composés cibles.


(3) Agent déshydratant et dessicant :
Dans les situations où l'eau doit être éliminée du système de réaction, LiNH2 peut agir comme agent déshydratant et dessicant pour assurer le bon déroulement de la réaction.
(4) Agents de déshalogénation et d'alkylation :
LiNH2 est également un catalyseur et réactif indispensable dans les réactions de déshalogénation et d’alkylation des hydrocarbures halogénés.
(5) Réactif d'aminolyse :
Dans la réaction d'ammonolyse, LiNH2 peut favoriser la réaction entre les réactifs et l'ammoniac, générant des produits d'ammonolyse correspondants.
2. Initiateur de polymérisation
LiNH2 peut également être utilisé comme initiateur pour la polymérisation anionique des composés éthyléniques, favorisant la réaction de polymérisation et synthétisant ainsi des composés polymères.
3. Synthèse de composés spécifiques
LiNH2 peut être utilisé pour fabriquer des composés spécifiques tels que des azides et des cyanures, élargissant ainsi sa gamme d'applications en synthèse organique.


Fabrication de médicaments
Dans l'industrie pharmaceutique, LiNH2 joue également un rôle important. C'est un catalyseur et une matière première importante pour la synthèse de divers médicaments.
1. Synthèse des vitamines
LiNH2 est un catalyseur important pour la synthèse de composés tels que la vitamine A et la vitamine D3. Grâce à son effet catalytique, ces vitamines essentielles à la santé humaine peuvent être synthétisées efficacement.
2. Catalyseur de synthèse de médicaments
Dans la production des antioxydants 1010 et 1076, LiNH2 est également utilisé comme catalyseur efficace pour la réaction d'alkylation des nitriles et des cétones. Ces antioxydants jouent un rôle important dans la synthèse et la conservation des médicaments.
Matériau de stockage d'hydrogène
Bien que LiNH2 lui-même libère de manière irréversible du NH3 lorsqu'il est chauffé, ce qui le rend impropre à une utilisation directe comme matériau de stockage d'hydrogène, en se combinant avec LiH ou d'autres matériaux de stockage d'hydrogène, il peut supprimer efficacement la libération d'ammoniac et présente une bonne réversibilité. Par conséquent, dans le domaine des matériaux composites de stockage de l’hydrogène, le LiNH2 présente un potentiel d’application important.


Utilisation en laboratoire
En laboratoire, LiNH2 est également couramment utilisé pour préparer d’autres composés ou mener des études de réactions chimiques spécifiques. En raison de ses propriétés chimiques uniques et de ses larges perspectives d'application, LiNH2 est devenu l'un des réactifs indispensables dans les laboratoires de chimie.

1) Chauffer du lithium métallique dans du gaz ammoniac peut produire une plus grande quantité deAmidure de lithium. Le lithium métal est placé dans une fine rainure en nickel, qui est ensuite placée dans un tube de verre. Le tube est incliné dans un four électrique et chauffé à 380-400 degrés. De l'ammoniac gazeux est introduit par une extrémité du tube et du LiNH2 fondu s'écoule de l'autre extrémité et se solidifie dans la section de refroidissement du tube de réaction. De cette manière, le lithium métallique peut exposer en permanence sa nouvelle surface, garantissant ainsi une réaction continue.
2) Empilez deux creusets en nickel l'un sur l'autre et placez-les dans un tube de verre vertical. Percez trois petits trous de 15 mm au fond du creuset en nickel ci-dessus. Lorsqu'il est chauffé à 400 degrés dans un flux d'ammoniac, le LiNH2 fondu peut s'égoutter en continu dans le creuset situé en dessous et se refroidir et se solidifier dans le flux d'ammoniac. LiNH2 est une substance cristalline incolore, transparente et brillante. Densité relative 1,178 (17,5 degrés). Point de fusion 380-400 degrés. Lorsqu'il est chauffé à 450 degrés sous vide, il peut se décomposer et libérer du gaz ammoniac et générer de l'imine de lithium. Li2NH se décompose en LiNH2 à 750-800 degrés.

Charles Hauser a utilisé pour la première fois LiNH2 comme base dans les années 1950 et 1960. L'aminolithium dans l'ammoniac liquide peut être utilisé pour préparer le lithium énol TBA, ainsi que dans diverses réactions de condensation aldolique de cétones et de substrats aldéhydes. Dans J Dans Org. Chem. 1960, 25, 503-507, Hauser a élargi son travail original pour inclure la réaction de l'énol lithium avec divers substrats cétones et aldéhydes, y compris l'acétate d'éthyle. Il existe des études utilisant LiNH2 comme base pour la réaction de condensation croisée de Claisen entre des structures couvrant l'énolate d'acétate de tert-butyle et des structures couvrant ECHB et HN, qui fait partie d'une longue liste comprenant des bases plus encombrées. La méthode décrite est une méthode avec un temps de réaction inférieur à 5 minutes. Cependant, il a été découvert que LiNH2 seul ne peut pas être utilisé efficacement comme base dans les réactions décrites dans la littérature technique existante, probablement en raison de sa faible solubilité.
Il existe également des études utilisantAmidure de lithiumdans l'ammoniac liquide pour la réaction d'autocondensation des esters de Claisen. Cependant, l'aminolithium dans l'ammoniac liquide est considéré comme inapproprié pour les réactions de condensation croisée de Claisen, en particulier pour les réactions de condensation de Claisen dans lesquelles un ou plusieurs esters contiennent des groupes hydroxyle. On pense que l’aminolithium dans l’ammoniac liquide déprotonne initialement le groupe alcool pour former de l’alcool lithium. Le lithium métallique de ce sel d'alcool est dans une position idéale pour se coordonner avec les groupes ester adjacents, et cette coordination améliore la réactivité de l'ester envers la substitution nucléophile.
Quels sont les effets secondaires de ce composé ?
Les effets secondaires de ce composé concernent principalement des risques potentiels pour la santé humaine et l'environnement. Voici une analyse détaillée de ses effets secondaires :
1.Effets secondaires sur la santé humaine
Toxicité aiguë
Contact avec la peau :
Il présente une forte irritation et une forte corrosivité pour la peau. Après contact, la peau peut présenter des symptômes tels que rougeur, gonflement, douleur et brûlure. Dans les cas graves, cela peut entraîner une nécrose cutanée ou des cicatrices permanentes.
Contact visuel :
Cette substance a également un fort effet irritant sur les yeux, ce qui peut provoquer des douleurs oculaires, des larmoiements, des rougeurs et même des lésions cornéennes ou la cécité.
Toxicité aiguë
Inhalation:
L'inhalation de vapeurs ou de poussières de cette substance peut provoquer une irritation des voies respiratoires, entraînant des symptômes tels que toux, respiration sifflante et difficultés respiratoires. Dans les cas graves, cela peut entraîner des maladies respiratoires telles qu'une pneumonie chimique et un œdème pulmonaire.
Ingestion:
Son ingestion accidentelle peut provoquer une érosion gastro-intestinale, entraînant des symptômes tels que des nausées, des vomissements, des douleurs abdominales et de la diarrhée. Dans les cas graves, cela peut mettre la vie en danger.
Effets d'une exposition à long terme-
Une exposition à long terme à ce composé peut entraîner un empoisonnement chronique et des dommages à plusieurs systèmes du corps humain. Cela inclut le système nerveux, le système respiratoire, le système digestif, le système reproducteur, etc. Les symptômes spécifiques peuvent varier en fonction des différences individuelles, mais incluent généralement des maux de tête, des étourdissements, une perte de mémoire, un manque de concentration, des difficultés respiratoires, une indigestion, une diminution de la fertilité, etc.
2.Effets secondaires sur l’environnement
Pollution atmosphérique
Lorsqu'il est exposé à des flammes nues, à une chaleur élevée et peut provoquer de fortes réactions chimiques au contact d'acides ou de substances oxydantes, il peut libérer des gaz toxiques. Si ces gaz sont émis dans l’air, ils pollueront la qualité de l’air et constitueront une menace pour la santé humaine.
Pollution de l'eau
La réaction avec l'eau ou la vapeur d'eau peut libérer des gaz toxiques ou inflammables et peut également produire des eaux usées nocives. Si ces eaux usées sont rejetées directement dans les plans d’eau sans traitement approprié, elles provoqueront une toxicité pour les organismes aquatiques et endommageront les écosystèmes aquatiques.
Pollution des sols
Les résidus présents dans le sol peuvent avoir un impact négatif sur les micro-organismes et les plantes du sol. Il peut inhiber l'activité des micro-organismes du sol, perturber l'équilibre écologique du sol et pénétrer dans le corps humain via la chaîne alimentaire après avoir été absorbé par les plantes, posant ainsi des risques potentiels pour la santé humaine.
3. Utilisation sûre et mesures de protection
Lors de l'utilisation, les procédures de sécurité doivent être strictement suivies pour garantir la sécurité du personnel et de l'environnement. Il doit être utilisé dans un environnement bien ventilé pour éviter une inhalation prolongée de vapeur ou de poussière. Évitez tout contact direct avec la peau et portez des vêtements de protection, des gants et des écrans faciaux appropriés lors de l'utilisation. Se laver les mains et le visage rapidement après utilisation pour éviter les irritations de la peau causées par les résidus.
Il doit être stocké dans un endroit frais, sec et bien ventilé, loin des sources de feu et de chaleur. Le récipient de stockage doit être bien scellé pour éviter les fuites et la volatilisation. Pendant le transport, des mesures anti-fuite doivent être prises pour garantir un transport en toute sécurité. Les véhicules de transport doivent être équipés du matériel -de lutte contre l'incendie et du matériel d'intervention d'urgence correspondant.
Lorsqu'une fuite ou un accident se produit, des mesures d'urgence doivent être prises immédiatement, comme évacuer le personnel, couper la source d'incendie et utiliser un équipement de lutte contre l'incendie approprié pour éteindre l'incendie. Le matériau qui fuit doit être immédiatement adsorbé avec des matériaux adsorbants tels que du sable et du charbon actif, et collecté dans un conteneur pour une élimination appropriée. Le personnel qui entre en contact avec des matériaux ayant fui doit immédiatement retirer les vêtements contaminés, se rincer la peau abondamment à l'eau et consulter un médecin dès que possible. Si le patient inhale accidentellement de la vapeur ou de la poussière, il doit être immédiatement amené à l'air frais, garder ses voies respiratoires dégagées et consulter un médecin dès que possible.
FAQ
A quoi sert l’amidure de lithium ?
Le lithium amide est un cristal ou une poudre incolore à gris avec une odeur d'ammoniac. Il est utilisépour fabriquer des médicaments, dans la fabrication de produits chimiques et comme catalyseur.
L'amide de lithium est-il une base forte ?
Les amides de lithium sont des composés très réactifs. Spécifiquement,ce sont des bases solides.
Quelle est la solubilité de l’amidure de lithium ?
La poudre d'amide de lithium est une poudre blanche avec un point de fusion de 375 degrés et un point d'ébullition de 430 degrés. C'estsoluble dans l'ammoniaque liquideet sa densité relative est de 1,178 (17,5 degrés).
La LDA est-elle une base forte ou faible ?
étiquette à chaud: lithium amide cas 7782-89-0, fournisseurs, fabricants, usine, vente en gros, acheter, prix, vrac, à vendre









